微分电化学质谱在锂离子电池研究中的应用
发布时间:2022-02-12来源:未知 编辑:admin
广告位置(首页一通--图文)
锂离子电池储能技术以其能量密度高、循环寿命长等优点,具有广阔的应用前景——从便携电子设备到电动车,直至大规模电网储能系统。锂离子电池主要由正负极、有机电解液和隔膜组成,通过Li+在正、负极间的可逆嵌入/脱嵌反应实现化学能和电能的相互转换,如图 1 所示。
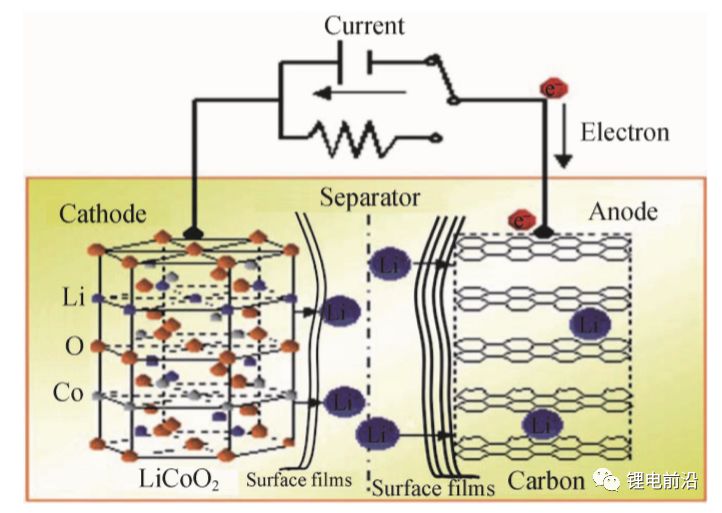
图 1 锂离子电池工作原理示意图
锂离子电池实际工作中,伴随上述可逆主反应,电解液与电极材料亦会发生诸多不可逆的副反应,其中最主要的是固态电解质界面膜理解SEI的形成机制是构筑高性能锂离子电池的关键步骤。传统的非原位手段无法直接从分子水平上解析SEI的形成机制,并且诸多非原位表征技术多在开放的环境下测试,会诱导 SEI膜发生物理或化学变化,降低测试准确性。相比于非原位技术手段,原位分析工具可以研究正在进行的物理化学过程、电池不同组件之间的相互作用、从空间和时间上给出SEI膜在形成过程中准确的动态变化信息,大大减小了实验误差。
1 发展历程
电化学质谱(electrochemical mass spectroscopy, EMS),是传统电化学与现代质谱分析技术的结合。在名称上,DEMS比 EMS多一个D(differential), 其有两方面的含义:
① DEMS可以测量所产生物种数量的时间导数(derivative),即形成速率;
② DEMS采用两级真空泵产生压力差(pressure difference)来输运气体产物。
对于DEMS来讲,它最重要部分就是一个“膜”将电池与质谱的真空系统分开,即进样方式。它必须满足两个要求:
第一 对于挥发物来说是可渗透的,电解液不可渗透。
其次 物种从电极界面到质谱检测器的转移时间(响应时间)要足够短。这样,电化学反应的时间或电势和质谱信号才能够完全匹配,实现真正意义的“differential”。
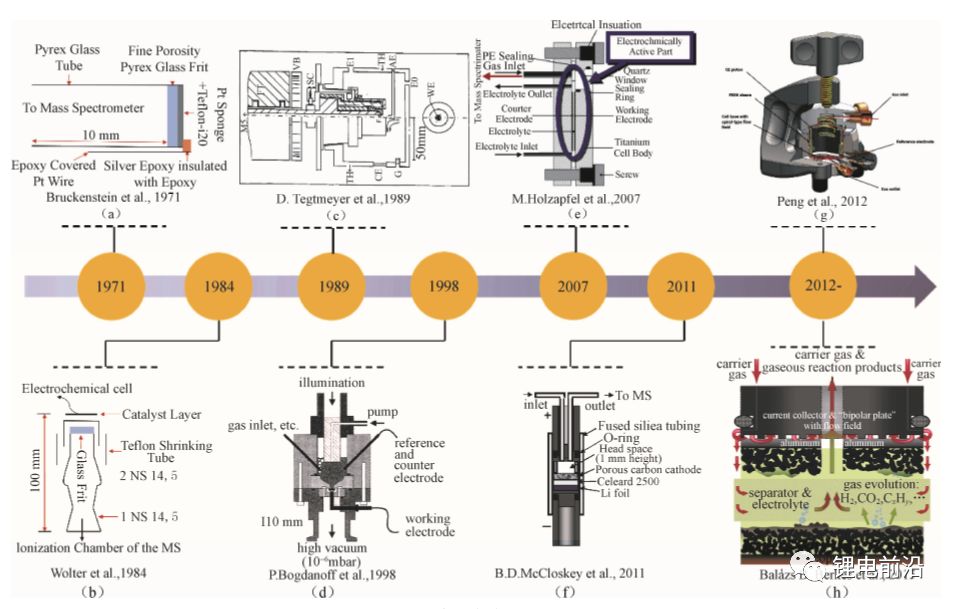
图 2 电化学质谱进样方式的发展历程
目前来看,载气吹扫进样方式使得气体的转移效率接近100%,定量结果较为准确。然而,DEMS的响应时间(一般在 1~5 s)远远不能达到单电子反应水平,比如飞秒级别,这样使得DEMS 研究多电子耦合的电化学过程变得尤为困难。此外,用DEMS直接研究实际锂离子电池体系还未见报道,比如圆柱、软包、铝壳电芯等。其中,几个技术难点需要克服:
① 实际的锂离子体系,如软包电池,化学/电化学产气量比质谱模型电池大很多,这也对DEMS的载气系统势提出了更高要求;
② 如何将实际的锂离子电池接入质谱的载气系统;
③ 气体定量准确性如何提高。
未来的研究方向将更多集中在 提高DEMS的时间分辨率,尽量缩短DEMS气路长度和毛细管管径以及尽可能增加载气流速或设计新型的进样方式。
2 DEMS体系
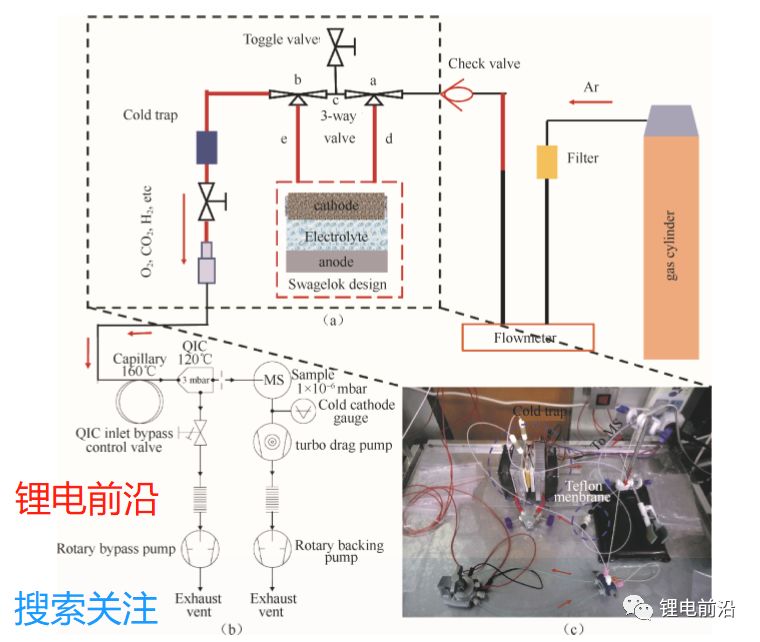
图 3 (a)DEMS 示意图;(b)质谱真空系统示意图;(c)载气系统和电化学反应装置数码照片
图3展示了DEMS系统的组成。主要部件是气体净化装置、流量控制器、电池单元、三通阀、可控温冷阱、电解液过滤膜和 PEEK管线。本节将着重介绍DEMS系统的组成、原理、实验流程、实验注意事项以及可能的误差等。
2.1 系统构成
2.1.1 载气系统
如图 3(a)和 3(c)所示,载气首先由气体钢瓶进 入气体净化装置,排除杂质气体(主要是 H2O 和 CO2 等)对实验的干扰,然后进入流量控制器。根 据实验体系的不同,质量流量控制器的流量设定通 常为 0.1~2 mL /min。
2.1.2 真空系统
不管早期的Teflon 膜进样或现代载气吹扫进样方式,其基本原理一致。
2.1.3 电池单元
相对于常规的锂离子测试电池,电化学质谱池的设计需要额外的进出气口,并且气密性需要严格保证。它的核心主要是气路设计,因为这决定了气 体传输效率和质谱定量的准确性。对于图 4(a)中的 气路设计,电化学/化学反应产生的气体依靠压力差(P0小于P1)扩散到载气中。这样的设计使得少部分气 体不能随载气到质谱中,而且同时形成一定的涡流,降低气体传输效率。此外,气体进入载气中使得载气压力突然(P2>P1)增加,这在一定程度上也会影响测试结果的准确性。在图 4(b)中,载气流进电解液组分,将电化学/化学反应产生的气体从电解液带入载气中。尽管这样的设计提高了气体的传输效率,但是也使得挥发性电解液大量进入载气中。如果测试时间过长,电解液会被耗干而迫使测试终止。另外,载气进入电解液会形成大量的涡流,可能使得电池系统不能趋于稳定状态。针对以上2种电池设计的弊端,图4(c)的电池气路设计,在电池上方形成螺旋梯度气体流场[见图2(g)三维示意图],使得气流更加稳定,大大减小了涡流情况的发生概率。此外,螺旋梯度流场也能增加气路长度,缓建载气 压力的骤然变化而且提高了气体传输效率。
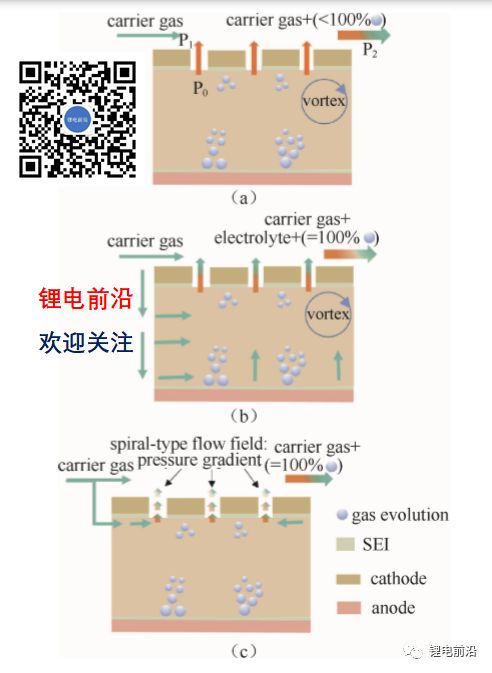
图 4 不同的电化学质谱池气路示意图
2.2 实验流程
首先,在DEMS研究锂离子电池副反应过程中,任何痕量杂质(如水、HF及少量空气等)都可能参与化学或电化学反应,影响测试结果的准确性。因此,电解质盐和溶剂必须在使用前进行纯化和干燥(除非这些试剂的纯度是电池级),以保证污染程度最小化。电解质锂盐应具有高纯度,一般需要达到 99.99%以上。对于纯度较低的电解质盐,重结晶过程是必不可少的一个步骤。对于达到电池级的锂盐,比如 LiClO4 和 LiPF6 不需要重结晶,但也需要在120℃真空干燥24h才可以使用。溶剂的种类和纯度与锂离子电池SEI膜的形成、锂离子的电导率、电池的安全性等有直接的关系。有机溶剂需要在配制电解液前进一步纯化和除水。对于高沸点溶剂,溶剂的纯化分为三个步骤。首先,将5g氢化钙(CaH2)加入到含有700mL溶剂的圆底烧瓶中,并将溶剂在室温下搅拌至少24 h以预先脱水。预脱水后,溶剂在真空密闭的条件下进行减压蒸馏。然后,将蒸馏溶剂直接从蒸馏装置中取出(不能暴露于空气),并转移到氩充满的 手套箱中。最后,用新鲜活化的3 Å(1 Å=1010m)分子筛进一步干燥蒸馏过的溶剂,这个过程至少需要3天以上。对于低沸点溶剂,纯化过程和高沸点溶剂相似,不同的是常压蒸馏即可。需要注意的是整个过程也应该在氩气氛下以避免空气污染。最终,纯化后的溶剂的水含量需要通过 Mettler-Toledo Karl Fischer 滴定仪测定,其最终含水量应小于10ppm。
2.3 电化学方法选择
在锂离子电池工作过程中,恒定电压和恒定电 流是两种常用的充放电方法。对于恒定电压模式,在充电初期充电电流会比较大,有可能造成电池温 度上升过快,对电池体系产生不利影响;对于恒定电流模式,在后期可能出现充电电流超过可接受电 流而导致电池电解液发生副反应(如析气反应)。若恒定电流太小,延长充电时间,降低充电效率,而且产气量太小可能会低于 DEMS 的检测限,因此,在DEMS实验中,需要选择合适的电化学方法以及参数(电流、电压)才能得到理想的实验结果。电化学反应速率取决于电极电位,循环伏安法(CV)已经被广泛应用于快速、定性和定量地给出电化学反应电位之间的关系。通常,循环伏安技术(经验地扫速0.1~1.0 mV/s), 可以确定电流密度,电位与消耗或释放气体速率之间的粗略关系。
3 DEMS在锂离子电池中的应用
锂电池的组件,包括正极、负极、电解液和隔膜等对电池的性能影响至关重要。尽管目前已经有大量先进的表征技术对锂电池进行了系统研究,提供了丰富的界面和物质结构变化等信息,但是它们都不可能原位检测并定量锂电池随电势变化的气体产物,以及电池的动力学信息。DEMS作为锂离子电池产气分析和安全性问题研究的强有力技术,它的研究进展已经在许多化学类顶级刊物上被报道。
3.1 电解液
丙烯碳酸酯(propylene carbonate,PC)作为一种锂离子电池广泛使用的电解液,几种可能的分解机制被提出。第一种可能分解机制是PC氧化开环形成丙酮或丙醛,伴随着CO2释放。另外一种分解机制认为PC分解产生CO2,丙醛以及顺式和反式-2-乙基-4-甲基-1,3-二氧戊环。接下来,以文献为例子,我们将解释如何用 DEMS 来验证PC可能的反应机制。DEMS测量中,根据可能的反应机制,首先要选择可能的电解液分解产物的质量数,通过扫描全谱(m/z = 0~300)得到。在所得质谱信号中寻找与离子电流或电位相关的质量数,独立的信号,即与离子电流和电位无关,便可以从反应机制中被排除。正如图 6(a)所展示,质量数58是与电位相关的信号。因此,它可以排除乙烷、乙烯、丙烷和丙烯的存在。这也就从实验角度验证了PC分解产生丙酮的分解机制。
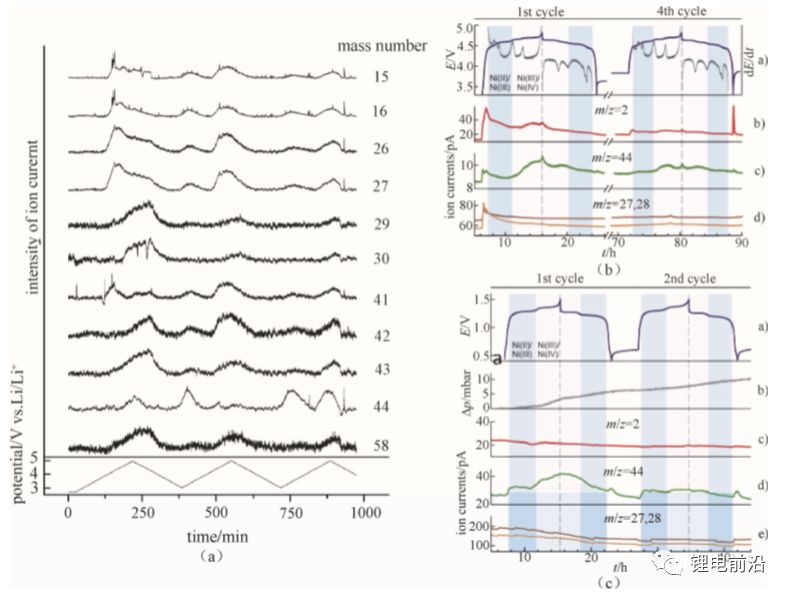
图 6 (a)离子电流随电位的变化曲线;(b)LNMO/石墨电池和 LNMO/LixFe1-xPO4电池(c)充放电曲线以及相应的 DEMS 信号
3.2 正极/负极-电解液界面
目前,锂离子电池中最具前景的正极材料是LNMO,最常用的负极材料是石墨。然而,它们的应用仍然存在一些限制,其中之一是 容量随循环而衰减,主要是由于过渡金属溶解和正 极或负极侧的电解质分解。理解LNMO/石墨电池的反应机制,将会支持锂离子电池系统的进一步发展。本节以 DEMS作为原位分析工具,分析讨论。LNMO/石墨电池的反应机制。以文献为例,首先,组装 LNMO|LiPF6- EC-EMC|石墨全电池[图 6(b)],4.57 V 和 4.64 V(vs. Li/Li+,后面提到的电位均相对于 Li/Li+)的充电平台分别对应于Ni2+到Ni3+和Ni4+的氧化,4.58V和 4.53 V的平台对应于充电的逆过程。在首圈充电阶段,m/z = 2、27、28和44的离子电流显著增加,由此推断电池充电过程产生氢(H2;m/z =2)、乙烯(C2H4;m/z =27、28)和二氧化碳(CO2;m/z =44) [图 6(c)]。首先,C2H4只有在充电初期才能被观察到,推断在石墨一侧可能涉及电解液分解,形成 SEI所致。然后,CO2在充电初期达到局部最大值,随后减小,最后在第二个充电平台(Ni3+=Ni4++e-)再次增加,整个放电过程中产气量最大值出现在约 4.58 V 的放电平台(Ni4++e-=Ni3+)处。二氧化碳不仅在高电压下释放,而且在较低电位也会释放,由此推断 CO2的释放可能包含两个途径。
第一,它是由电解质的分解或表面分解产物产生的。
第二,当镍离子处于中间电荷状态(Ni3+)时,大量的 CO2 释放。这表明 Ni3+对电解液氧化过程有一定的催化作用。
最后,H2的释放总体行为与CO2相似。这表明这两者之间存在相关性,可能涉及正极表面电解质组分的氧化和与分解产物如 HF 之间的反应。
3.3 添加剂
除了正负极和电解液之外,电解液添加剂对于改善锂离子电池寿命至关重要。在首次充电过程中,添加剂可优先于电解质分解,形成稳定的SEI层,极大较少了电解质的消耗以及可燃性气体的释放。本节将以DEMS为例,来说明它在甄别添加剂方面的应用。碳酸亚乙烯酯(vinylene carbonate, VC)由于较好的热稳定性,是目前研究最广泛的锂离子电解质添加剂之一。首先,组装石墨/LixFe1-xPO4电池(若研究Li负极,则组装 Li/LixFe1-xPO4电池)。然后,执行空白试验,当没有添加剂时,检测前几圈(SEI形成通常在前几圈)释放气体种类(如 C2H4、CO2、H2等)并定量,计算气体释放速率。最后,电解液加入不同含量 VC(一般要低于5%)时,观察气体释放含量是否减少,如使用EC电解液时,通常观察C2H4是否减少。当气体释放总量以及释放速率最小时,得出最佳的添加剂使用比例。
4 DEMS与其它先进技术的联用
电解质和电极之间的界面(主要是SEI),保持健康性对电池性能和安全性方面起着极其重要的作用。原位分析能够判断电池的健康状况以及诊断电池问题的根源。如前文所述,DEMS可以监测和识别和计算由于界面反应而产生的气态物质。然而, DEMS单一分析技术不能提供一次理解界面现象的所有所需信息,如界面的组成、形貌、力学和电学性质。如果用不止一种原位技术分析电池体系,即分批处理,可能会导致某些人为处理错误,并使处理时间耗费。因此,将各种原位工具集成在一起有助于对锂电池界面进行全面有效分析。
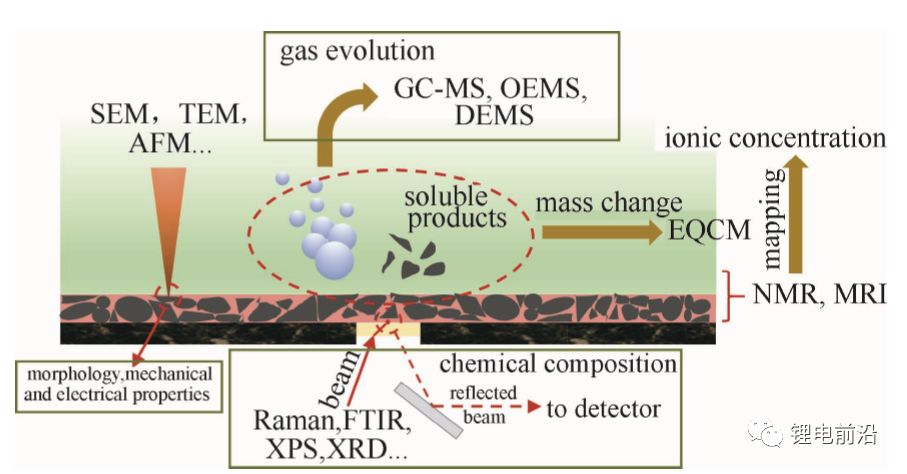
图 7 电极-电解质界面集成分析工具
5 结 语
尽管 DEMS 提供了锂离子电池界面反应气体相关的独特信息,但我们并不否认其它原位工具在研究SEI界面的重要作用。开发 DEMS以及与DEMS集成互补的联用技术将有利于深入剖析锂离子电池的界面反应机制和其它电化学器件的微观结构研究,如锂空气电池、锂硫电池、锌空气电池、镁电池和钠电池等。
参考文献:微分电化学质谱:研究锂离子电池的一项关键技术 作者赵志伟 ,彭章泉