浅谈锂离子迁移数的提高与锂离子电池快充
发布时间:2021-12-27来源:未知 编辑:admin
广告位置(首页一通--图文)
电动汽车产业的快速发展对锂离子电池的快充能力提出了更高的要求,目前针对快充电池的设计更多针对的是电极结构的改进,例如采用倍率性能更好的正负极材料、降低电极涂布量、降低压实密度等方法,这些方法已经为锂离子电池的快充性能带来了很大的提升。但是目前大家对提升Li+在电解液中的迁移系数关注的还不是很多。在充放电的过程中,正负极之间的电场会推动阴阳离子在正负极之间进行迁移(Li+带正电荷,会在电场的作用下向负极进行迁移,阴离子,如PF6-带负电荷,会在电场的作用下向正极迁移),所以电解液的电导率是由阴阳离子共同组成的(所以高电导率并不一定意味着Li+迁移效率高),但实际上只有Li+的迁移对我们来说才是有意义的,因此我们定义Li+的迁移数量占电解液中所有的离子迁移数量的比例为Li+的迁移数,如下式所示。

从上式我们可以看出,Li+的迁移数t+越接近1,那么电解液中迁移的Li+占比就越高,那么电解液在正负极之间传递电荷效率就会越高。但是目前商用的锂离子电池电解液采用为LiPF6电解质盐,因此虽然它们具有很高的电导率(1-10mS/cm),但是它们的Li+迁移数却都在0.5以下,这也就是说大多数的电导率都是由阴离子PF6-提供的,因此电解液的电导率的意义也就大打折扣了。造成这一现象的原因主要是因为Li+溶解在电解液中时会发生溶剂化,从而在其表面产生一层溶剂化的外壳,从而限制了Li+的迁移速度,而阴离子几乎不会发生溶剂化。
这就产生了一个问题——过多的阴离子聚集在正极表面,在正负极之间产生了一个浓度梯度,这会使得锂离子电池产生一个浓差极化,导致较大的过电势,限制了锂离子电池能量密度和功率密度的提升。研究显示,当Li+的迁移数提高到约0.7左右,就能显著的提升锂离子电池的快速充电能力,因此如何在高的电导率s下,保持高的迁移系数对于提高锂离子电池的功率密度和能量密度具有重要的意义。
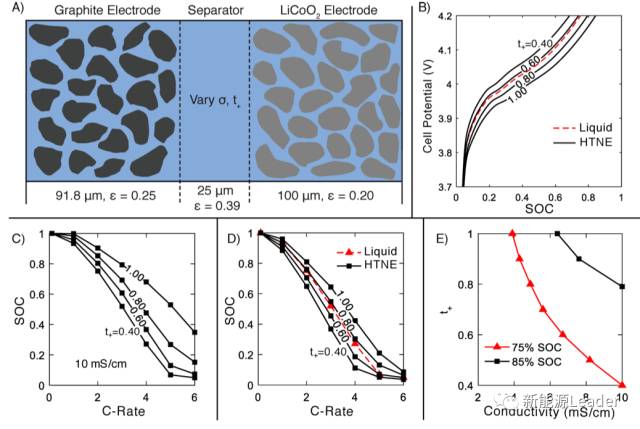
为了检验Li+迁移数对锂离子电池性能的影响,美国加州大学伯克利分校的Kyle M. Diederichsen利用有限元模型对一个由多孔石墨负极、多孔LiCoO2正极做成的电池模型(如上图a所示)进行了分析(实验中的对照组为液态电解液,其Li+迁移数t+约为0.4,电导率约为10mS/cm)。
从上图b中可以看到,随着Li+迁移数的提高,电池在充电过程中的过电势(极化)明显降低,而从图c和d中可以看在较高的充电倍率(2-6C)下,具有高的Li+迁移数的电池最终充入的电量要明显高于低迁移数的电池,这表明高的Li+迁移数能够有效的提高锂离子电池的快速充电能力。接下来我们来看看图E的数据,即在2C的充电倍率下,要获得75%和85%的SoC,在不同的电导率下,需要多大的Li+迁移数,从曲线可以看到Li+迁移数越大,那么相应的需要的电解液电导率也就越低,如果Li+的迁移数达到0.8,那么相比于液态电解液对电导率的要求能够下降50%。
既然电解液的Li+迁移数如此重要,为何大多数电解液厂商仍然使用电导率来表征电解液呢?这是因为相比于成熟的电导率测试方法,电解液Li+的迁移数的测量要困难的多,特别是在电解液中阴阳两种离子都在扩散时,这让Li+迁移数的测量变的困难重重,并且准确率较低,这也是目前大多数厂家没有采用Li+迁移数表征电解液的重要原因。
当然,测量困难不代表着没有方法,测量Li+迁移数目前最广泛使用的办法是Bruce and Vincent方法,该方法的原理是首先测量在锂离子电池刚刚开始的电流IO(此时电解液仍然非常均匀),在稳定一段时间后,测量稳定电流ISS,我们假设此时正负极之间阴离子净通量为0,如果忽略掉正负极和电解液的一些副反应,那么此时的电流ISS都是由Li+进行传导的,因此我们有t+=ISS/IO。但是该方法还存在较大的局限性,首先是该方法只在低浓度电解液中有效,并且还需要排除掉电解液在正负极发生的副反应。
最近Balsara和Newman通过加入Newman数对上述方法进行修正,获得了更加准确的Li+迁移数。当然其他测试电解液中的Li+迁移数的方法还很多,只是他们大多数都过于复杂,因此目前大多数的研究者仍然假设电解液是一种稀溶液,从而简化测量过程。
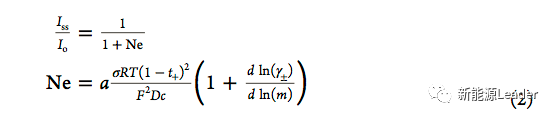
在上文中我们主要探讨了电解质的Li+迁移数与锂离子电池快充性能之间的关系,伯克利分校的Kyle M. Diederichsen的研究成果让我们对提高Li+迁移数的重要意义有了深刻的认识,接下的内容中继续对如何提高电解质的Li+迁移数进行进一步的探讨。
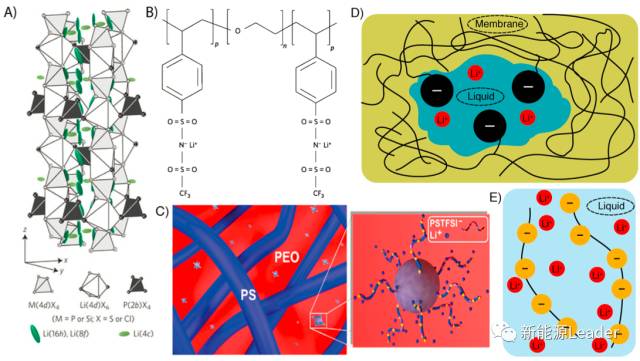
从上文的介绍中我们也可以看到,开发Li+迁移数更高的电解液对于快充电池的意义不言而喻,实际上这一项研究也在持续进行,例如下图中的Li+导体陶瓷材料就是一种单离子导体,因此其迁移数为1。图b中的固体聚合物电解液通过将阴离子固定在聚合物的骨架结构上,避免了阴离子的迁移,提高了Li+的迁移数。为了提高上述的共聚物电解液的性能,人们还向其中添加了小分子溶剂和纳米颗粒,如图d所示。另外一种思路是固定液体电解液中的阴离子,例如采用工具阴离子、高浓度电解液等方法提高液体电解液的Li+迁移数。
上述提高电解质Li+迁移数的方法也都有各自的优点和局限性,那么接下来我们就和大家一起进行以下分析。
-
陶瓷基单离子导体
固体氧化物电解质是近年来研究非常火热的一种陶瓷基的单离子导体,目前研究比较火热的主要是石榴石相的金属氧化物材料,例如Li7La3Zr2O12,以及锂硫代硫酸盐,Li2S−P2S5等,这些材料本身具有很高的离子电导率,在室温下最高可达25mS/cm,同时这些电解质中只有Li+能够进行迁移,因此是一种非常理想的电解质候选者。但是陶瓷电解质要真正的应用在锂离子电池上还面临很多挑战,首先是由于陶瓷材料的脆性很强,因此在制成厚度小于100um,甚至是20um的电解质膜的工艺就非常难以实现。同时传统的固相合成方法会在陶瓷电解质内形成众多的晶界和微孔,从而极大的降低陶瓷电解质的电导率(实际中陶瓷电解质因为晶界电阻的存在,锂离子电导率要远低于理论值)。
-
单聚物电解质
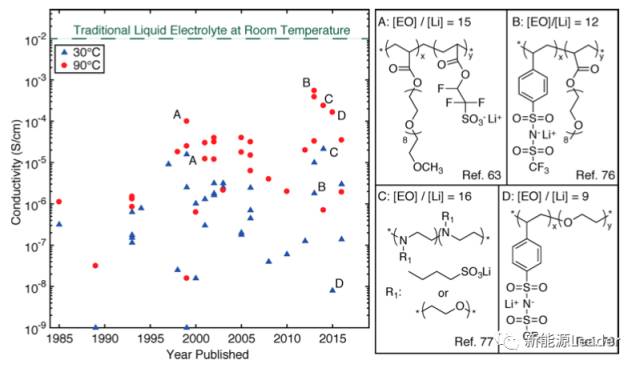
在这中电解质中,阴离子被固定在一个聚合物长链上,因此不会在电场的作用下发生移动,因此Li+的扩散只能以占据空位的形式进行,这也导致了这种电解液中Li+的扩散速度要明显低于液体电解质,从而使得其在室温下电导率很低。下图总结了自1985年首次发现单离子导体聚合物电解质以来,不同聚合物电导率在30和90℃下电导率提升情况(根据不同年份发表论文整理)。从图上可以看到在过去的20年中单离子导体聚合物电解质常温电导率一直维持在10-5S/cm左右,鲜有提升
-
添加剂改性聚合物电解质
鉴于单离子导体聚合物电解质的性能提升非常困难,人们尝试向其中添加少量的小分子溶剂和纳米颗粒来改善其电导率。小分子溶剂的主要作用是提高Li+的溶解度,从而提高电解质中载流子的浓度。向聚合物电解质中添加一定数量的纳米颗粒也能够有效的提高电解质的电导率,例如相PEO/LiCiO4中添加部分TiO2能够显著改善电解质的电导率。最近的研究显示,通过向聚合物电解质中添加部分添加剂可以在Li+迁移数高于0.9的情况下,将电导率提高到10-4S/cm。未来关于聚合物电解质的研究应该聚焦在深入理解“添加剂-盐-聚合物”之间的反应机理上。
-
液体电解质
液体电解质是目前锂离子电池上主流的电解液选择,因此如何提高液体电解质的Li+迁移数,是我们最为关心的内容。液体电解质的电导率一般能够达到10mS/cm,远远高于其他类型的电解质,但是由于Li+溶剂化外壳的限制,Li+迁移数一般都低于0.5,这也极大的限制了采用液体电解质的锂离子电池的快速充电的能力。解决这一问题可以通过两个方面着手,首先可以从限制阴离子的移动着手,例如在2013年Archer等人就提出了将阴离子固定在纳米颗粒上的思路,另外一个思路就是利用高浓度的锂盐实现,例如高浓度的LTFSI的电解液的Li+迁移数就可以达到0.7,研究认为这可能是独特的溶液结构使得阴离子的移动能力大大降低,而阳离子受到的影响则较小。
总的来说,我们目前在提高液态电解质方面所作的工作还比较少,因此这方面还有很广阔的前景。加州大学伯克利分校的Kyle M. Diederichsen认为可溶性的聚合物阴离子锂盐是实现高Li+迁移数液态电解质的有效途径,值得我们在这方面进行深入研究。
