锂电池中Li+扩散系数的测定方法
发布时间:2023-12-19来源:未知 编辑:admin
广告位置(首页一通--图文)
锂电池中Li+扩散系数的测定:恒电位间歇滴定法(PITT)
PITT是一种测定DLi+的方法。该方法以无限快动力学和半无限厚线性系统为边界条件,由电流响应I(t)对电位阶跃ΔE(1~10mV)得到扩散系数,具体公式如式(1):

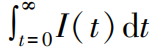 ,为平衡时初始电位和末端电位之间转移的电荷数。经近似和变换,可得式(2)、(3):
,为平衡时初始电位和末端电位之间转移的电荷数。经近似和变换,可得式(2)、(3):
式(2)、(3)中:I0为电流(I)的初始值;L为电极上活性物质的厚度;Z为活性物质的得失电子数;F为法拉第常数;S为工作电极的活性物质与电解质接触的电化学活性表面积;c0、cs分别为Li+的初始浓度和阶跃后的浓度。
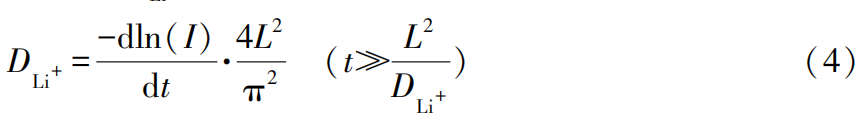
锂电池中Li+扩散系数的测定:电化学阻抗谱法(EIS)
电化学阻抗谱(EIS)法
EIS法根据平面电极的半无限扩散阻抗模型及Fick第一定律和Fick第二定律等推导出DLi+。具体推导如下。根据平面电极的半无限扩散阻抗模型可知,Warburg阻抗Zw可表示为:

对于Fick第二定律,结合Fick第一定律、EIS测试条件的阻抗计算式和Butler-Volmer方程,可得到Warburg系数σ的计算公式:
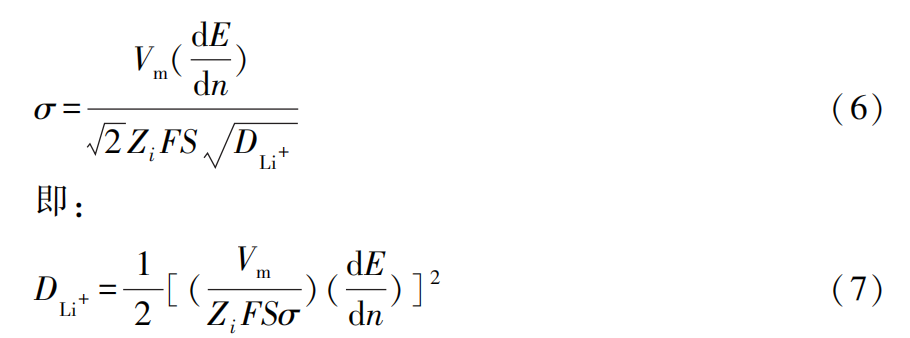
式(7)中:Vm为活性物质的摩尔体积;E为开路电位;n为活性材料中的嵌锂量;Zi为扩散离子所带电荷数。
EIS技术相较于其他电化学方法最大的不同,是可以得到Li+在电极界面电荷转移电阻的内扩散系数,而PITT、CITT、GITT和CV等电化学方法没有考虑颗粒内部结构和复合电极的电荷转移电阻,求得的DLi+是表观扩散系数。EIS还可以通过不同的频率范围,区分电极过程电化学反应的速率控制步骤。这意味着即使速率控制步骤不是电极内部扩散过程,采用EIS仍能有效地得出结果。
L.P.Teo等[1]以锂和锡的乙酸盐为原料,采用溶胶-凝胶法制得Li2SnO3,用作锂离子电池负极材料,用EIS测得DLi+为10-12~10-14cm2/s。C.M.Cholant等[2]采用掺杂MoO3的方法来改善V2O5薄膜在电化学领域应用时的一些缺点(如DLi+低、电导率低、材料循环性能不理想等),利用EIS测得掺杂后的薄膜DLi+明显改善,达到10-10 ~10-12cm2/s,证明MoO3/V2O5薄膜的应用潜力。应注意的是,EIS只适应于阻抗谱平面图上有Warburg阻抗的情况,且需要的参数较多,如Vm、n和S等。如何精确获取这些参数,将直接影响最终结果的准确性。
参考:周肇国, 徐艳辉. 锂离子电池中Li+扩散系数的测定方法[J]. 电池, 2022, 52(2):5.
[1] Teo L P , Buraidah M H , Arof A K . Study on Li + ion diffusion in Li 2 SnO 3 anode material by CV and EIS techniques[J]. Molecular Crystals and Liquid Crystals, 2019, 694(1):117-130.
[2] Cholant C M , Azevedo C F , Caldeira I , et al. Li+ ions diffusion coefficient in V2O5:MoO3 Sol-Gel films[J]. Molecular Crystals and Liquid Crystals, 2017, 655(1):61-70.
锂电池中Li+扩散系数的测定: 恒流间歇滴定法(GITT)
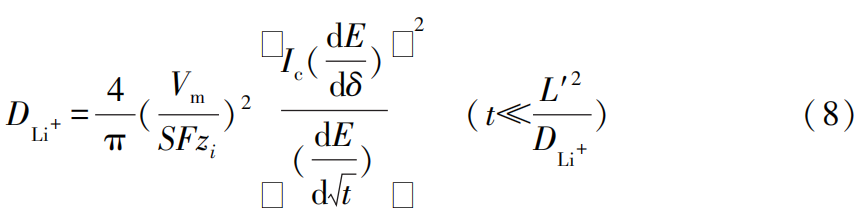
式(8)中:zi为电子转移数;Ic为外加恒电流;δ为初始化学计量偏差;L′为扩散距离。GITT是目前测定DLi+所用最主要的方法,操作简单、数据准确,也是测定DLi+的标准方法。
K.Chudzik等[1]在研究LiMn2O4正极材料中掺杂K、S成分对电化学性能的影响时,用溶胶-凝胶法合成了4种不同掺杂情况的Li1-xKxMn2O4-ySy(x:y=1:1、1:2、1 :3和2:1),通过GITT测得DLi+在10-11~10-9cm2/s数量级,并且随着S含量的增加而降低。这表明S含量过高会降低材料导电性,从而限制Li+迁移率。
姚停等[2]在研究前驱体形貌对锂离子电池正极材料LiFePO4的电化学性能的影响时,利用GITT测定了3种样品制备的LiFePO4的DLi+,结果显示多孔颗粒状的样品的DLi+最高,证明了存在微观孔隙的前驱体制备的LiFePO4的Li+嵌脱速率更高。吕桃林等[3]为深入研究LiNi0.5Mn1.5O4电极材料,建立了变固相扩散系数(VSSD)模型,对材料的放电过程进行模拟。利用该模型和GITT分别测定LiNi0.5Mn1.5O4放电过程中的DLi+,发现结果基本一致(10-15cm2/s),证明了VSSD模型的可行性。
GITT和EIS一样,参数需要较高的精确性。另外,在低温下,随着温度的降低,电荷转移电阻增大、双层电容充电时间延长,大量的锂扩散使得相应的Li+扩散通量随着时间的延长逐渐增大,违反了一般GITT模型扩散问题的边界条件,导致GITT结果出现偏差。基于此,T. Schied等[4]提出了一个描述恒流脉冲期间电位变化的模型,以改进低温GITT扩散分析。A. Nickol等[5]在-40~40℃的温度下,基于NCM523正极材料,研究了有关GITT的理论及实验分析,提出可以将GITT和EIS互补使用,以提高低温下测定DLi+的准确性。
参考:周肇国, 徐艳辉. 锂离子电池中Li+扩散系数的测定方法[J]. 电池, 2022, 52(2):5.
[1] Chudzik K , Witosawski M , Bakierska M , et al. Electrochemical properties of K and S doped LiMn2O4 studied by GITT and EIS[J]. Electrochimica Acta, 2021.
[3吕桃林,罗英,晏莉琴,等 . LiNi0.5Mn1.5O4电极的变固相扩散系数模拟[J]. 电池,2017,47(2):84-89.
[5]GITT Analysis of Lithium Insertion Cathodes for Determining the Lithium Diffusion Coefficient at Low Temperature: Challenges and Pitfalls[J].
锂电池中Li+扩散系数的测定: 循环伏安法(CV)
循环伏安法(CV)

式(9)中:IP为峰值电流;R为理想气体常数;T为温度;v为扫描速度。
CV是目前最常用的电化学技术之一,测定DLi+的操作简单,对于数据处理,只需绘出IP和v1/2的关系曲线,根据式(9)即可求得DLi+。T.T.D.Tran等[1]在研究LiFePO4/C纳米复合电极材料的电化学性能时,基于CV求得DLi+为2.2×10-12cm2/s,与其他文献报道的由CV、GITT和EIS测得的数据一致。
CV法虽能较简易地得到DLi+,但得到的是充放电过程中的平均扩散系数。由于CV过程中浓度变化较大,基于该技术确定扩散系数的可靠性较差。此外,CV只能快速而粗略地估计扩散系数的数量级,因此,很多研究者为了实验的完整性,多采用CV辅助观测氧化还原峰,以研究电化学反应的机理,DLi+则用其他方法,如 EIS计算得出。
C.J.Lyu等[2] 在研究Nb掺杂对一维纳米结构NCM正极材料的影响时,通过CV观察到Nb-NCM的氧化峰和还原峰电位差均小于NCM,证明掺杂Nb可提高库仑效率,缓解电化学极化。通过EIS计算,得出Nb-NCM的DLi+为1.8×10-10cm2/s,大于NCM的1.13×10-12cm2/s,表明Nb掺杂有利于Li+的迁移。
参考:周肇国, 徐艳辉. 锂离子电池中Li+扩散系数的测定方法[J]. 电池, 2022, 52(2):5.
[1] Huynh L T N , Tran T T D , Nguyen H H A , et al. Carbon-coated LiFePO4–carbon nanotube electrodes for high-rate Li-ion battery[J]. Journal of Solid State Electrochemistry, 2018.
[2] Cl A , Jing Y A , Yi P A , et al. 1D Nb-doped LiNi 1/3 Co 1/3 Mn 1/3 O 2 nanostructures as excellent cathodes for Li-ion battery[J]. Electrochimica Acta, 2019, 297:258-266.
锂电池中Li+扩散系数的测定: 容量间歇滴定法(CITT)
CITT是通过引入电位-电荷容量与电流-电荷容量之比(RPG),在此基础上发展起来的、连续测定DLi+的方法。具体推导如下。
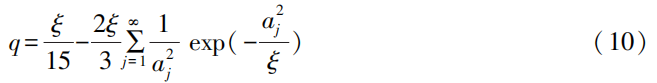
式(10)中:ξ为定义的无因次变量,取值为r2/DLi+tG;tG为恒流充电时间;aj为常数列。
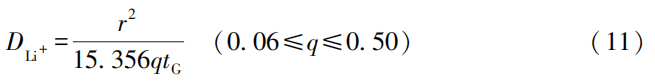
CITT的优势在于数据处理相对简单。其他测试方法需要许多互补的参数,包括活性材料组成、嵌锂量、有效表面积和摩尔体积等,而CITT只要测试出r、q和tG,即可得到DLi+。q和tG可由CITT循环曲线求得,因此只用测定r,即可求得DLi+;CITT还可连续确定不同充电状态和不同循环情况下的DLi+ 。
S.Y.Wang等[1]利用KMnO4控制氧化MnCO3前驱体与锂盐的固相反应,制备LiMn2O4固相微球和壁厚可调节的空心微球,在研究结构对LiMn2O4作为锂离子电池正极材料性能的影响时,通过CITT测得样品LMO-3、LMO-5和LMO-S(LMO-y,y指KMnO4与MnCO3反应的时间,min;S指固相微球)的DLi+在10-11~10-8.5cm2/s数量级,且LMO-3数值最大,证明壁厚较薄的LMO-3的Li+迁移率更高。
王盈来等[2]合成NCM粉末正极材料,利用CITT测得,DLi+随电位和循环次数的不同分布于10-12~10-11.5 cm2/s;电位在3.9~4.3V时,DLi+较为稳定;循环次数越多,DLi+越稳定。事实上,,相比于其他电化学方法,尽管CITT处理数据更简单,但更多的学者仍倾向于使用 EIS、GITT等这些经过实践且更为成熟的方法,因此,CITT 实际运用并不广泛。
参考:周肇国, 徐艳辉. 锂离子电池中Li+扩散系数的测定方法[J]. 电池, 2022, 52(2):5.
锂电池中Li+扩散系数的测定: 电位阶跃法(PSCA)
电位阶跃法(PSCA)
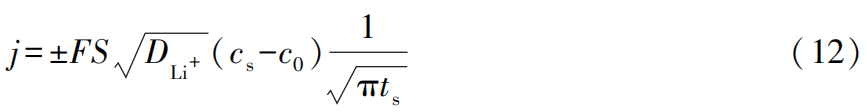

PSCA法的优势在于操作简单,同时数据处理较简单。数据处理时,只需要记录电位阶跃过程中暂态电流j随ts-1/2的变化,求得斜率即可。
C.W.Liu等[1]采用悬浮混合法制备TiN改性的LiFePO4/C,利用PSCA测得各样品LFP/C、TiN-4、TiN-5和TiN-6(TiN-z中z指质量分数z%的TiN包覆LFP/C)的DLi+分别为7.01×10-6cm2/s、9.43×10-6cm2/s、22.00×10-6cm2/s和16.5×10-6cm2/s,即含5% TiN的样品表现出最佳的电化学性能。
此外,一些学者还采用了双电位阶跃(DPSC)法,相比PSCA,DPSC会在短时间内施加两个阶跃,使之前的电极反应产物回到原始状态,更有利于动力学分析。B. Gélinas等[2]研究基于三酰亚胺阴离子和2,5-二叔丁基-1,4-二甲氧基苯(DDB) 的电活性离子液体(RIL)作为Li4Ti5O12/LiFePO4锂离子电池过充保护添加剂的电化学性能,采用DPSC测定含10mmol/L 3-(2,5-二叔丁基-4-甲氧基苯氧基) 丙基磺酰 ( 三氟甲基磺酰) 亚胺 ([MIm] [DDB-pNTf])和 4-叔胺-丁基-2,5-二甲氧基苯基磺酰(三氟甲基磺酰)亚胺([BMIm] [MDB-NTf])的锂离子电池电解液的DLi+,分别为0.48×10-6cm2/s和0.47×10-6cm2/s。
参考:周肇国, 徐艳辉. 锂离子电池中Li+扩散系数的测定方法[J]. 电池, 2022, 52(2):5.
[1]LIU C W, AN J, GUO R S, et al. Enhanced electrochemical per- formance of LiFePO4/C cathode material modified with highly con-ductive TiN[J]. J Alloys Compd,2013,563:33-38.
[2]B Gélinas, Bibienne T , M Dollé, et al. Electroactive ionic liquids based on 2,5-ditert-butyl-1,4-dimethoxybenzene and triflimide anion as redox shuttle for Li4Ti5O12/LiFePO4 lithium-ion batteries[J]. Journal of Power Sources, 2017, 372:212-220.