2019年诺贝尔化学奖授予了John B. Goodenough、M. Stanley Whittingham和Akira Yoshino,以表彰他们对锂离子电池发展做出的贡献,这项技术彻底改变了我们的生活方式。在此,我们回顾一下具有里程碑意义的重大发现(这些发现已经塑造了现代锂离子电池),以提供启发性的见识并指导未来的突破。
可充电锂离子电池已经转移到了便携式电子设备,并且是电动汽车的首选技术。它们使间歇性可再生能源更深入地渗透到电力系统中,以在未来实现更可持续的方面发挥着关键作用。现代锂离子电池由两个电极组成,通常是钴酸锂(LiCoO2)正极和石墨(C6)负极,它们由浸入非水系液体电解质中的多孔隔膜相隔开,该隔膜含有LiPF6在碳酸亚乙酯(EC)和碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、碳酸乙基甲基酯(EMC)至少一种线性碳酸酯组成混合液和许多添加剂的电解液。在充电过程中,锂离子从LiCoO2晶格结构移动到负极侧,形成锂化石墨(LiC6)。在放电期间,这些离子回到CoO2主体框架,而电子则释放到外部电路。正是这种穿梭过程或所谓的摇椅化学改变了我们的现代生活。
锂金属是最轻的金属,具有高的比容量(3.86 Ah g-1)和极低的电极电位(-3.04 V vs 标准氢电极),使其成为高电压和高能量电池的理想负极材料。然而,Li+/Li的电化学电势高于实际已知非水系电解质的最低未占据分子轨道(LUMO),导致电解质不断还原,形成钝化的固体电解质界面(SEI)[1]。由于大的体积变化和锂金属的高反应活性,SEI容易遭到损坏并在锂金属表面进行不均匀的修复,从而导致枝晶的生长,这可能导致电池短路并着火(图1a)。
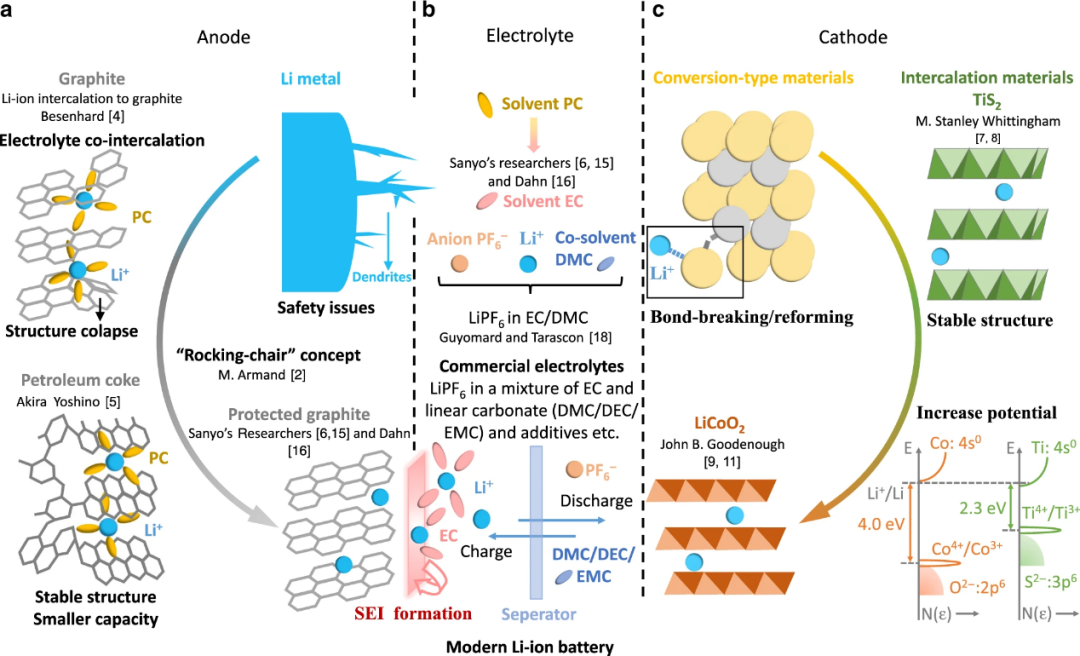
图1:里程碑式的发现塑造了现代锂离子电池。(a)包括锂金属、石油焦和石墨等负极材料的开发;(b)具有溶剂碳酸亚丙酯(PC)、碳酸亚乙酯(EC)和至少一种选自碳酸二甲酯(DMC)、碳酸二乙酯(DEC)、碳酸乙基甲基酯(EMC)和许多添加剂混合溶剂组成的电解质;(c)正极材料,包括转化型材料、插层材料二硫化钛(TiS2)和钴酸锂(LiCoO2)。
为了避免锂金属的安全问题,Armand建议使用两种不同的嵌入主体来构造锂离子电池[2,3]。Besenhard报道了第一个基于石墨电极的锂离子嵌入,显示石墨可以嵌入包括锂离子在内的几种碱金属离子[4]。基于具有垂直平面的半-填充Pz轨道,层状结构石墨能够嵌入锂离子。该平面可以与Li 2s轨道相互作用,从而限制体积膨胀和枝晶生长。但是,石墨的比容量(LiC6,0.372 Ah g-1)[1]比锂金属的要小得多。直到发生数起火灾事故,Moli Energy公司全面召回锂金属电池后,越来越多的石墨等插层材料被视为是替代锂金属以提高安全性的可行负极。当时,电解质(碳酸亚丙酯PC)的共嵌入导致石墨剥落和塌陷(图1a),这对石墨在电池中的应用带来了挑战。
1985年,旭化成公司的Akira Yoshino[5]发现,石油焦(石油馏分残余物中石墨化程度较低的物质)可以以~0.5 V(Li+/Li)的低电势可逆地嵌入锂离子,而不会破坏结构。它的结构稳定性源自石油焦中的无定形碳区域,该区域用作将各层固定在一起的共价接头[6](图1a)。尽管与石墨(~Li0.5C6,0.186 Ah g-1)[6]相比,石油焦的无定形性质限制了容量,但由于其循环稳定性而成为第一个商用的锂离子电池插层负极。
为了满足锂金属的高容量需求,首先考虑了包括金属氟化物、硫化物或氧化物在内的转化型正极(图1c)。在电池工作期间,这些材料会反应形成具有不同结构和新成分的相[6]。因此,转换型电极不允许进行多次循环,因为在每次循环期间都会发生键的断裂和重整。
认识到转化反应的局限性后,科学家们转向了新的锂离子存储机制,该机制在循环过程中不会发生结构塌陷。Whittingham及其同事在埃克森美孚公司(Exxon)[7]开发的层状结构金属硫属化物(MX2)备受关注,因为它们具有可存储锂离子客体的空间。他们发现二硫化钛(TiS2)可以在整个化学计量范围内以最小的晶格碰撞来化学地嵌入锂离子。在1973年和1974年,Whittingham将TiS2用作电池的正极(图1c),随后在1976年展示了2.5 V的电池[8]。
显然,TiS2//Li电池的低电压表明其能量密度受到限制。为了找到可以在较高电压下嵌入锂离子的新型正极材料,Goodenough求助于金属硫属元素化物(MX2,X = O)的氧化物当量。他指出,S-3p[6]谱带的能量上限比O-2p[6]谱带的高,这使金属氧化物的嵌入电压高于金属硫化物[9](图1c)。金属硫化物中S-3p[6]谱带的较高能量归因于较小的Madelung静电能(较大的硫化物离子),以及在无限分离下将电子从阳离子(Mn+)转移到S-/S2-所需的更大能量[9]。
这种基本认识导致Goodenough及其同事发现了三类氧化物正极[10]。在1979年和1980年,Goodenough报道了一种钴酸锂(LiCoO2)[11],它可以在电压高于4.0 V vs Li+/Li下可逆地吸收和释放锂离子,并且与锂金属负极结合使用时可实现4.0 V的可充电电池。然而,钴的丰度有限,对其应用构成了成本壁垒。具有四面体-位锂离子的尖晶石LiMn2O4[12]氧化还原电位为〜4.0 V,并且具有较低的成本。然而,由于电解质中存在的H+离子(ppm级)使得Mn溶解而导致的降解问题限制了它的应用。与Fe2O3/Fe3O4等简单的氧化物相比,聚阴离子型氧化物LixFe2(XO4)3(X == S、Mo、W等)[13,14]提供了更高的电池电压。聚阴离子型氧化物中的共价X-O键通过诱导作用削弱了Fe-O键的共价性,从而导致Fe2+/3+对的氧化还原能量降低,从而氧化还原电位增加(如从Fe2O3中的<2.5 V到LixFe2(SO4)3的3.6 V)。聚阴离子型氧化物具有降低成本的优势,并由于氧的紧密共价键结合而提高了热稳定性和安全性。但是,它具有差的电子导电性和较低的密度。迄今为止,在这三类氧化物中,具有高质量和体积能量密度的层状氧化物仍然是最受欢迎的正极[10],而LiCoO2电极现在是为大多数个人电子设备供电的主要正极材料。
电解质的工作窗口取决于其LUMO和最高占据分子轨道(HOMO),其应分别高于负极的电化学势(μa)和低于正极的电化学势(μc)(LUMO > μa ,HOMO < μc)。或者,在LUMO < μa或HOMO > μc的情况下,应分别在负极或正极上形成稳定的钝化SEI层[1]。
通过调整电解质成分来构建稳定的SEI可实际应用于石墨负极。最初,PC比碳酸亚乙酯(EC)更加可取,因为PC的熔点(-48.8 ℃)比EC的更低(36.4 ℃)[6]。然而,据报道,PC会引起石墨的结构破坏,从而导致较差的循环寿命。Sanyo的研究人员[6,15]声称在EC-基电解质中成功进行了石墨的电化学锂化处理,Dahn[16]报道到,EC可以通过牺牲SEI的形成来抑制石墨剥落,为锂离子电池石墨负极的开发铺平了道路(图1b)。从那时起,EC成为锂离子电池必不可少的溶剂。“ EC-PC差异”[17]的潜在机制归因于其还原产物之间的差异。碳酸亚丙基锂(PC的还原性产物)的弯曲链结构易于在电极表面形成疏松的沉积物,并具有较弱的内聚力。EC倾向于在Li+溶剂化壳层中形成石墨插层化合物(具有大的阴离子,如PF6-),从而导致形成更多含F的SEI产物,其LUMO和HOMO之间的能带大到足以隔离来自负极的电子隧穿,使电解液分解得到有效钝化。
旭化成公司组装了一块完整的可充电电池,该电池将石油焦负极与Goodenough开发的LiCoO2正极结合在一起,后来在1990年由索尼公司实现商业化(〜80 Wh kg-1、200 Wh L-1)(图1)。Sanyo的研究人员[6,15]的发现和Dahn的工作(EC作为共溶剂)[16]为开发具有石墨负极的锂离子电池铺平了道路,并将电压和能量密度分别提高到4.2 V和400 Wh L-1。在1993年,Guyomand和Tarascon[18]报道了一种新的电解质配方——LiPF6在EC/DMC,以提高其氧化稳定性(图1b)。直到今天,这种电解质仍然是最受欢迎的电解质之一,其提供LiCoO2锂离子电池的能量密度(250 Wh kg-1,600 Wh L-1)是索尼[3]第一代设备的三倍。
这些里程碑式的发现都不是凭空出现的。后期的成功通常取决于先前的知识和进步。Walter Rüdorff早在1965[19]年就观察到TiS2可以容纳锂离子的现象,但直到1973年,Whittingham[7]才将这种层状二硫化物用作锂电池的正极。然后,TiS2//Li的消亡鼓舞了Goodenough来研究层状氧化物,以设计具有较高电极电势的正极。同样,在20世纪70年代[4],石墨被报道嵌入锂离子,但直到Sanyo研究人员[6,15]的工作和Dahn[16]引入共溶剂EC才开始得以应用。此举是基于对降解机制的深入了解。对这些突破是如何产生的反思能够使我们理解到跨学科研究的至关重要性。
尽管具有高反应活性和枝晶问题,但在20世纪70年代至80年代期间,使用锂金属负极是自然选择。呼吁使用由Armand[2,3]制成正极和负极的不同插层材料或由Yoshino[5]开发的石油焦替代锂金属,尽管表面上看似追求高能量电池,但事实证明,这是实现可充电锂离子电池商业化的必要步骤。这些发展鼓励我们秉持开放态度,敢于挑战现有的颠覆性创新电池设计智慧。
锂离子电池的影响范围将超越便携式电子产品,而影响到社会可持续发展的领域。为了满足对电气化运输和大规模储能解决方案不断增长的需求,不断的材料开发和突破性的化学方法将成为锂离子电池在充分提高成本效益、功率和能量密度和安全方面全部潜力的关键。
通讯作者:香港中文大学卢怡君教授(Yi-ChunLu)教授
Xie, J., Lu, Y. A retrospective on lithium-ion batteries. Nat Commun 11, 2499 (2020).
DOI: 10.1038/s41467-020-16259-9