锂电综述:电池中的可逆热效应及其计算方法
发布时间:2021-09-22来源:未知 编辑:admin
广告位置(首页一通--图文)
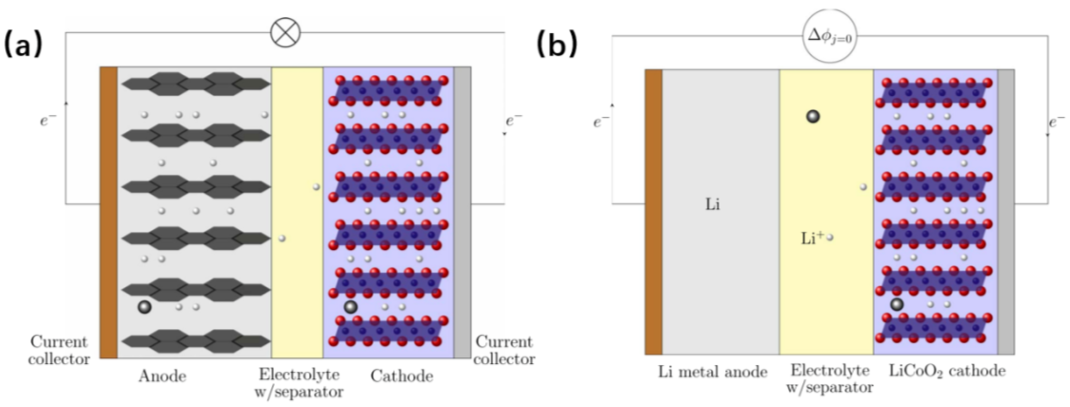
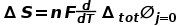
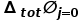 是电池电流为0时的电动势,即开路电压E。等式(1)适用于全电池和半电池。
是电池电流为0时的电动势,即开路电压E。等式(1)适用于全电池和半电池。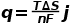
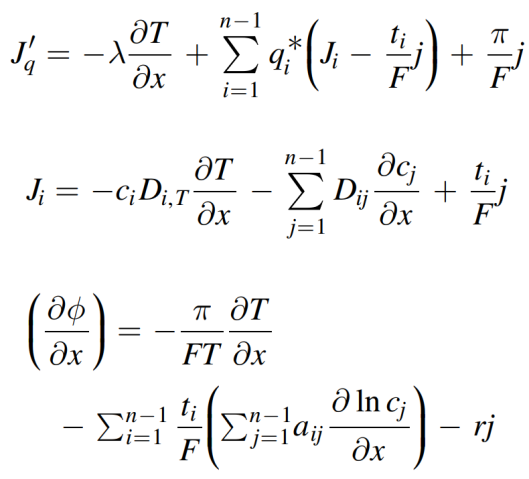
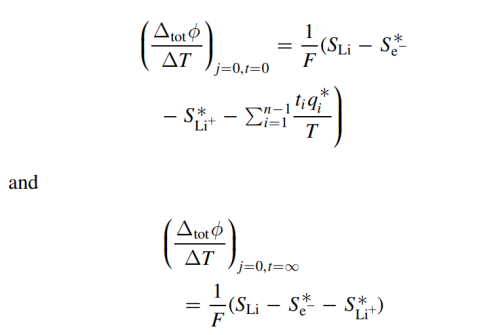
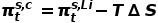
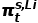 是在任何状态t下锂阳极的珀耳帖热。此公式适用于稳态和初始状态。金属电极的初始状态珀耳帖热随电解质类型的变化不大。因此,阴极的珀耳帖热的变化只与电荷状态或温度的变化与ΔS有关。
是在任何状态t下锂阳极的珀耳帖热。此公式适用于稳态和初始状态。金属电极的初始状态珀耳帖热随电解质类型的变化不大。因此,阴极的珀耳帖热的变化只与电荷状态或温度的变化与ΔS有关。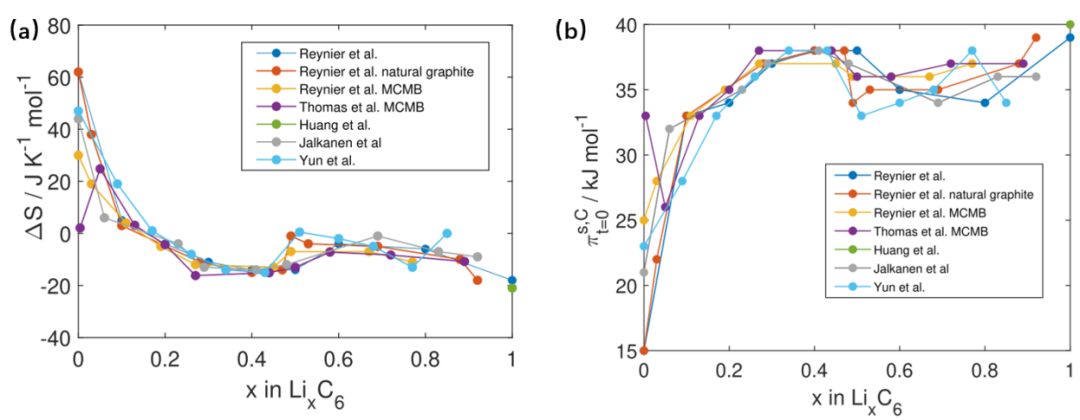
发布时间:2021-09-22来源:未知 编辑:admin
广告位置(首页一通--图文)

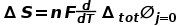
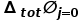 是电池电流为0时的电动势,即开路电压E。等式(1)适用于全电池和半电池。
是电池电流为0时的电动势,即开路电压E。等式(1)适用于全电池和半电池。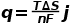

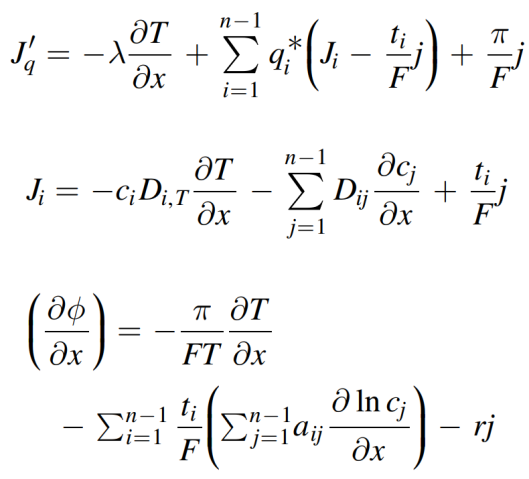
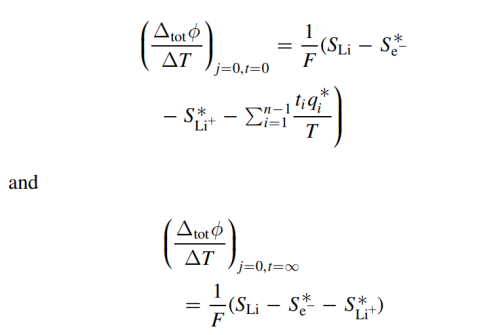
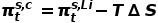
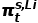 是在任何状态t下锂阳极的珀耳帖热。此公式适用于稳态和初始状态。金属电极的初始状态珀耳帖热随电解质类型的变化不大。因此,阴极的珀耳帖热的变化只与电荷状态或温度的变化与ΔS有关。
是在任何状态t下锂阳极的珀耳帖热。此公式适用于稳态和初始状态。金属电极的初始状态珀耳帖热随电解质类型的变化不大。因此,阴极的珀耳帖热的变化只与电荷状态或温度的变化与ΔS有关。